|
透射电镜取材注意事项生物样品透射电镜取材注意事项 取材是电镜实验的第一步,其操作成功与否直接关系到电镜结果的效果 及成败。为了得到好的结果,请务必按要求做好取材!取材基本要点:快 (1min)、冷(4 ℃)、小(1 mm3)、净(无杂质)、准(部位准确)。不 同的样品,取材细节上有很大区别,有任何疑问,请扫描右方二维码,即可 获得专业一对一电镜实验及解图指导! 一、动物组织取材流程及要求 取材流程:动物麻醉或断头急性处死,解剖取出所需的器官或组 织,生理盐水简单冲洗血液及组织液。按要求将组织切成1mm3左 右小块,固定于组织及细胞电镜专用2.5%戊二醛固定液。 取材要求: 1、位置:肝、肺、脾等无需定位组织取1mm3组织,3-5块;需要定位组织如骨骼肌、肾、肠、血管、胰岛等组织取材大小为0.5mm× 1mm×3mm左右的长条状,且保证观察结构在组织块中。 2、操作:试剂、容器、器械提前4℃预冷;组织离体后,1min内浸 入戊二醛固定液。取材时,可提前准备一个载玻片(硬卡纸),滴 几滴戊二醛固定液,把标本浸在液滴中修整至合适大小(时间可稍 长),用牙签挑出 3~5 粒标本,放入1.5ml尖头EP管。将修整好的 标本块放入戊二醛固定液后,普通 4℃冰箱保存。
二、细胞取材流程及要求 取材流程:细胞直接刮下(不可胰酶消化,会造成细胞损伤),细胞 悬液离心,弃上清,PBS 洗2次(敏感的细胞直接固定,不洗),低速 (1000-3000rpm)离心成团,加入组织及细胞电镜专用2.5%戊二醛固定 液 4℃过夜后快递。悬浮细胞、菌液可直接视为细胞悬浮液操作。固体 培养基培养的菌可直接将菌落挑到PBS中,后续操作一致。 取材要求: 1、细胞数量充足(6cm 或10cm 皿长满),离心后在ep管中绿豆大小; 2、缓冲液、戊二醛固定液等PH值7.3-7.4,4℃提前预冷; 3、贴壁细胞连着培养基用细胞刮斜着快速刮下,不要反复来回刮; 4、细胞悬液转入离心管,1000-3000rpm离心成团,弃上清,加PBS,将细胞转入1.5ml尖头 ep管,再次离心后弃上清。再加PBS重复上述步骤,最后加2.5%戊二醛固定,4℃保存。操作 轻柔,尽量保证细胞不散开。(转速及时间请结合细胞情况,尽量低转速、短时间,以细胞 离心成团为准!(PBS 清洗时间过长,易造成细胞损伤); 三、植物组织取材及要求 取材流程:PBS冲洗样品,确保无泥沙等污染物。然后用锋利刀片或剪刀将 样品切成合适大小,装入预冷的植物及细菌电镜专用2.5%戊二醛中。不需要定位的样品切成1立方毫米大小(如叶片、果实、花粉等),需要定位的 样品,切成0.5mm×1mm×3mm的长条状(茎、根、表皮等)随后抽气,让组织能沉淀到管底。(简易抽气方法:将植物组织同固定液一起倒入注射器, 用乳胶手套食指堵住注射器出口,右手拉动针栓,将注射器口垂直向上, 松开食指,右手轻推针栓使液面上的气泡从注射器口排出,反复多 次,直 至组织沉入固定液。)
四、其他样品 悬浮细胞、细菌可视为细胞悬液操作。固体培养的细菌,可视为被切小的组织块,直接用牙 签挑取3-5个菌落即可。外泌体、纳米材料、脂质体、病毒颗粒等负染样品,根据样品特 点,固定或不固定后合适条件运输。具体可咨询工作人员。 五、样本储存运输标准: 储存:样本取材后,4℃保存时间不超过1个月。 运输:固定液充满EP管,封口膜封口,气泡膜或报纸包裹厚一些。最后泡沫盒+冰袋 的方式运输,冰袋2-3个(-20℃冰袋,不要太多),一定要与样品隔开。特殊样品 如脂肪、植物等,用纱布将样品压到液面以下,保证充分固定。(下图1)
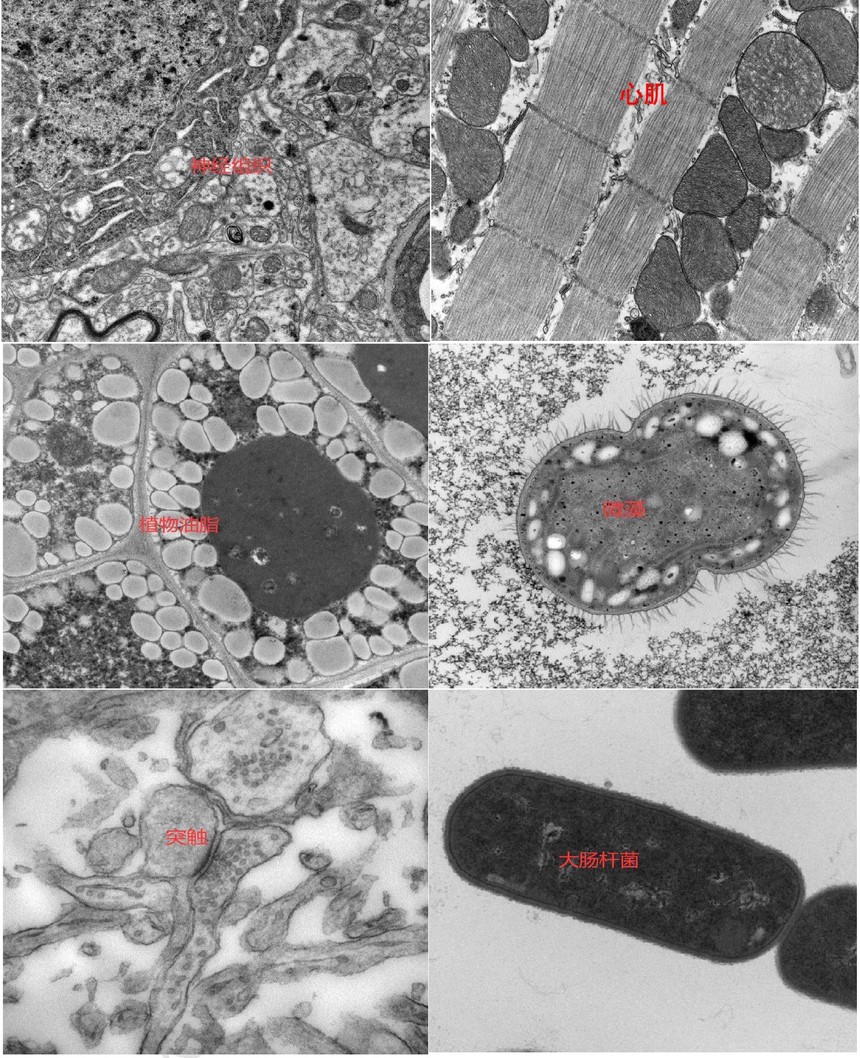
六、邮寄地址: 电话号码:刘振 18317038349 业务邮箱:biofcen@163.com 地址:湖北省武汉市洪山区高新四路 40 号葛洲坝.太阳城 18 栋304-1(北 1) 部分例图展示:
|